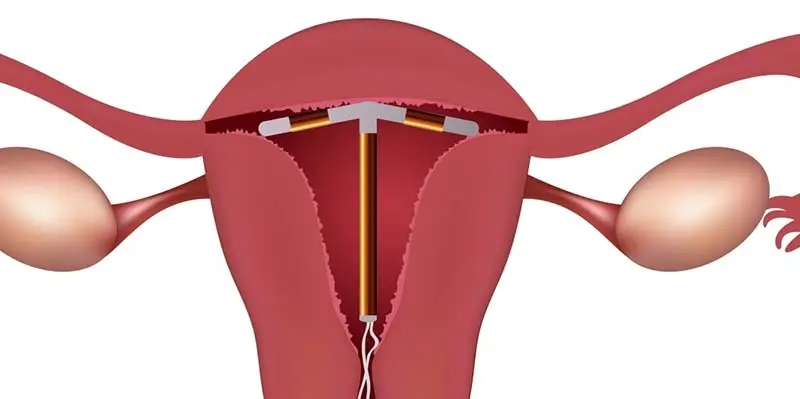
Pierwotne bolesne miesiączkowanie jest jednym z najczęstszych zaburzeń ginekologicznych u dorastających dziewcząt i kobiet. Odnosi się do nawracającego i skurczowego bólu występującego w dolnej części brzucha i talii bez zdiagnozowanej choroby organicznej. Według badań epidemiologicznych, częstość występowania PDM u kobiet w wieku dojrzewania wynosi 40–80%, a 15% kobiet w wieku reprodukcyjnym cierpi na ciężką postać PDM, która poważnie wpływa na jakość ich życia. Zazwyczaj dolegliwości pojawiają się tuż przed miesiączką (24–48 godzin) lub po jej wystąpieniu, a swoje największe natężenie osiągają w ciągu pierwszych 48 godzin. Bóle miesiączkowe mają charakter bólów skurczowych zlokalizowanych w dole brzucha, często promieniujących do krzyża lub ud. Wśród objawów towarzyszących do najczęstszych należą: bóle kolkowe, bóle głowy, nudności, wymioty, uczucie ogólnego rozbicia, biegunka, zaburzenie równowagi oraz labilność nastroju. Niekiedy bolesne miesiączkowanie poprzedza zespół napięcia przedmiesiączkowego charakteryzujący się obrzękiem, stwardnieniem i bólami piersi, depresją lub wzmożoną pobudliwością. Z badań statystycznych wynika, że jest to prawdopodobnie najczęstsza pojedyncza przyczyna nieobecności młodych kobiet w pracy i w szkole. Często wiąże się z ciężkimi stanami depresyjnymi. Mimo tak częstego występowania, etiopatogeneza tego zespołu chorobowego nadal pozostaje niewyjaśniona i jest przedmiotem wielu kontrowersji w piśmiennictwie medycznym [1–5].
REKLAMA
Etiologia pierwotnego bolesnego miesiączkowania
Szczególną rolę w powstawaniu PDM przypisuje się prostaglandynom. Badania wykazały, że etiologia PDM wynika ze zwiększonego nieprawidłowego skurczu macicy spowodowanego nadmierną produkcją i wydzielaniem prostaglandyn w macicy, w szczególności: prostaglandyny F2α (PGF2α), prostaglandyny E2 (PGE2), 6-keto-prostaglandyny F1α (6-keto-PGF1α, stabilny metabolit prostacykliny) i tromboksanu B2 (TXB2, metabolit z TXA2). Obecnie wiadomo, że są to hormony działające miejscowo, syntetyzowane m.in. w endometrium, ale również w ścianie naczyń i myometrium. Prostaglandyny są metabolitami przemiany kwasu arachidonowego (ARA) pod wpływem cyklooksygenazy (COX) i nie są magazynowane w tkankach, a ich synteza ma miejsce bezpośrednio przed uwolnieniem. Prostaglandyny PGF2α i TXA2 są silnymi stymulantami czynności skurczowej macicy, powodują napięcie macicy, a co za tym idzie – zmniejszony przepływ krwi, który może sprzyjać zakrzepicy. Działanie przeciwne wykazuje prostaglandyna PGE2 oraz prostacyklina – PGI2, gdzie PGE2 rozluźnia macicę poprzez hamowanie skurczów i spontaniczną aktywność mięśni gładkich, a prostacyklina – PGI2 łagodzi objawy PDM poprzez rozszerzanie naczyń krwionośnych, zapobiegając agregacji płytek i zakrzepicy. Mechanizmy regulujące biosyntezę prostaglandyn nie są do końca poznane. Wśród elementów pobudzających syntezę i uwalnianie prostaglandyn wymienia się czynniki nerwowe, serotoninę, acetylocholinę, histaminę, adrenalinę, angiotensynę II, bradykininę oraz estrogeny, które wzmagają syntezę prostaglandyn w endometrium. W badaniach klinicznych zaobserwowano, że w endometrium i krwi miesiączkowej kobiet z PMD występuje znacznie podwyższony poziom prostaglandyn PGF2α i TXB2 oraz niższe wartości 6-keto-PGF1α i PGE2 w stosunku do grupy zdrowych kobiet. Na tej podstawie podwyższone wartości PGF2α i 6-keto-PGF1α uznano za wskaźniki diagnostyczne w PDM [1, 2, 6, 7].
Wśród innych czynników mogących wpływać na zwiększone napięcie mięśnia macicy można wymienić działanie wazopresyny i oksytocyny. W etiologii PDM nie udało się udowodnić czynników natury behawioralnej i psychologicznej, uważa się je raczej za zjawisko wtórne w przebiegu schorzenia. Mniejszą rolę przypisuje się też obecnie udziałowi zmian anatomicznych, szczególnie w obrębie szyjki macicy, gdzie nie stwierdzono różnic w szerokości kanału szyjki macicy i cieśni u kobiet z PMD w porównaniu do kobiet zdrowych [7, 8].
Niewyjaśnione mechanizmy oraz wielorakość czynników biorących udział w etiopatogenezie PDM wskazują na konieczność prowadzenia dalszych badań dotyczących tego zagadnienia.
Leczenie pierwotnego bolesnego miesiączkowania
Sposób leczenia PMD powinien być dobrany indywidualnie, w zależności od natężenia dolegliwości bólowych, potrzeb pacjentki w zakresie regulacji płodności oraz pod względem współistniejącej choroby. Ze względu na wzmożoną syntezę prostagladyn w błonie śluzowej macicy, lekiem pierwszego rzutu są inhibitory syntezy prostaglandynowej (ISP) – niesteroidowe leki przeciwzapalne (NLPZ). Kobiety, u których występuje zapotrzebowanie na antykoncepcję, bądź nie reagują lub nie tolerują leków z grupy ISP, a u których nie ma przeciwwskazań do antykoncepcji hormonalnej, preferowaną terapią są doustne środki antykoncepcyjne [9].
Liczne badania naukowe wskazują, że dwuskładnikowa antykoncepcja hormonalna zawierająca CMA stanowi jeden z podstawowych elementów leczenia bolesnego miesiączkowania. W najnowszych klinicznych badaniach Roth i wsp. na temat porównania wpływu CMA, dienogestu (DNG) i drospirenonu (DRSP) na biosyntezę prostaglandyn w modelu ludzkich eksplantatów endometrium wykazano, że CMA w porównaniu do DNG i DRSP ma silniejszy efekt supresyjny na mRNA COX-2 (ryc. 2) i uwalnianie PGF2α stymulowane przez IL-1β – jako modelu bolesnego miesiączkowania. W całej kohorcie 31 eksplantów poziomy tkanek mRNA COX-2 i uwalnianie PGF2α były istotnie zwiększone przez IL-1β, a efekt ten był znacznie zmniejszony przez CMA (ryc. 3). Efekty DNG i DRSP były istotne tylko dla ekspresji mRNA COX-2, ale nie dla uwalniania PGF2α. Otrzymane wyniki odpowiadają obserwacjom klinicznym i potwierdzają, że CMA jest skutecznym lekiem na bolesne miesiączkowanie [10].
Kolejnym istotnym badaniem potwierdzającym skuteczność produktu medycznego zawierającego CMA jest badanie przeprowadzone przez Sabatini i wsp.


w ludzkich eksplantatach endometrium (źródło: [10])

w ludzkich eksplantatach endometrium (źródło: [10])

miesiączkowanie w okresie 12 cykli (źródło: [12])

u kobiet z bolesnym miesiączkowaniem (źródło: [12])
W tym prospektywnym badaniu obserwacyjnym porównywano działanie dwóch preparatów zawierających 30 μg etynyloestradiolu w połączeniu z 2 mg CMA lub 3 mg DRSP. Badaniem objęto grupę 156 aktywnych seksualnie nastolatek w wieku 14–19 lat. Młode kobiety przez okres 6 miesięcy przyjmowania preparatu medycznego (po 3 cyklach i po 6 cyklach przyjmowania preparatu) były obserwowane m.in. pod względem oceny bolesnego miesiączkowania.
Przed rozpoczęciem badania 64,2% (N = 104) cierpiało z powodu bolesnego miesiączkowania. Co ciekawe, tylko w grupie CMA odnotowano postępującą i znaczącą redukcję bolesnego miesiączkowania, która trwała do końca obserwacji (CMA vs DRSP: p < .01). Tę samą tendencję stwierdzono w przypadku bolesnego miesiączkowania (CMA vs DRSP: p < .01). Otrzymane wyniki badań potwierdzają skuteczność obu preparatów, które zapewniły skuteczną antykoncepcję, dobrą kontrolę cyklu i korzystny wpływ na wcześniej istniejące choroby skóry, bez wpływu na masę ciała. Warto jednak zauważyć, że po 3 cyklach osiągnięto korzyści dla obu grup, ale korzyści później wzrosły tylko w grupie CMA. Trwałe działanie CMA można wytłumaczyć jego chemicznym i farmakologicznym podobieństwem do naturalnego progesteronu [11].
Inne długofalowe badania, prowadzone przez okres 12 cykli, również potwierdzają powyższe wyniki. Zahradnik w swojej pracy dowiódł, że dwuskładnikowa antykoncepcja hormonalna zawierająca 0,03 mg etynyloestradiolu oraz 2 mg octanu chlormadynonu o nazwie Belara jest nowoczesnym i skutecznym środkiem antykoncepcyjnym, który leczy dolegliwości bólowe związane z PDM oraz oferuje szereg dodatkowych korzyści pozaantykoncepcyjnych. Badacz wykazał, że po zastosowaniu leku Belara na grupie 1266 pacjentek cierpiących na PDM objawy ustąpiły w 66% przypadków, a ból związany z miesiączkowaniem uległ zmniejszeniu o kolejne 13% po 12 cyklach stosowania leku Belara [12].
| Baza wyjściowa | Cykl 3 | Cykl 6 | p | ||||
| DRSP | CMA | DRSP | CMA | DRSP | CMA | ||
| Długość cyklu | 29 ±5 | 30 ±6 | 29 ±4 | 29 ±2 | 29 ±3 | 29 ±1 | |
| Długość krwawienia | 5 ±3 | 5 ±4 | 4 ±2 | 4 ±1 | 4 ±2 | 4 ±1 | |
| Krwawienie międzymiesiączkowe | 30 (38,4) | 32 (41,0) | 21 (26,9) | 14 (17,9) | 18 (23,1) | 9 (11,5) | .001* |
| Bolesne miesiączkowanie | 48 (61,5) | 56 (71,7) | 23 (29,3) | 18 (13) | 20 (25,6) | 10 (14,1) | .01* |
W dalszym badaniu na grupie 1939 kobiet z częstymi bolesnymi miesiączkami, które stosowały inne środki antykoncepcyjne, wystąpił prawie 95-procentowy spadek bolesnych miesiączek po 4 cyklach stosowania leku Belara (ryc. 5) [12].
W powyższych badaniach wykazano, że preparat medyczny Belara zawierający 0,03 mg etynyloestradiolu oraz 2 mg CMA jest niezawodnym i skutecznym doustnym środkiem antykoncepcyjnym w leczeniu bolesnego miesiączkowania. Działa w mechanizmie bloku wydzielania enzymów stanu zapalnego (fosfolipazy A2 oraz COX2) oraz ścieńcza endometrium, co pływa na redukcję poziomu prostaglandyn. Przekłada się to na zmniejszenie skurczów macicy, dając efekt redukcji bólu u pacjenta [11]. Belara to produkt odpowiedni dla wszystkich grup wiekowych.
Piśmiennictwo
- Cheng Y., Chu Y., Su X. i wsp. Pharmacokinetic-pharmacodynamic modeling to study the anti-dysmenorrhea effect of Guizhi Fuling capsule on primary dysmenorrhea rats. Phytomedicine. 2018; 48: 141–151.
- Benedetto C. Eicosanoids in primary dysmenorrhea, endometriosis and menstrual migraine. Gynecol Endocrinol 1989; 3: 71–94.
- Zahradnik H.P., Breckwoldt M. Contribution to the pathogenesis of dysmenorrhea. Arch Gynecol 1984; 236: 99–108.
- Gagua T., Tkeshelashvili B., Gagua D. i wsp. Assessment of anxiety and depression in adolescents with primary dysmenorrhea: a case-control study. Journal of pediatric and adolescent gynecology 2013; 26: 350–354.
- Petraglia F., Parke S., Serrani M. i wsp. Estradiol valerate plus dienogest versus ethinylestradiol plus levonorgestrel for the treatment of primary dysmenorrhea. Int J Gynaecol Obstet 2014; 125: 270–4.
- Nguyen A.M., Humphrey L., Kitchen H. i wsp. A qualitative study to develop a patient-reported outcome for dysmenorrhea. Quality of Life Research 2015; 24: 181.
- Kim S.A., Um M.J., Kim H.K. i wsp. Study of dienogest for dysmenorrhea and pelvic pain associated with endometriosis. Obstet Gynecol Sci 2016; 59: 506–11.
- Jabbour H.N., Kelly R.W., Fraser H.M. i wsp. Endocrine regulation of menstruation. Endocr Rev 2006; 27: 17–46.
- Zahradnik H.P., Hanjalic-Beck A., Groth K. Nonsteroidal anti-inflammatory drugs and hormonal contraceptives for pain relief from dysmenorrhea: a review. Contraception 2010; 81: 185–96.
- Roth K., Zahradnik H.P., Schäfer W.R. Effects of different progestins on prostaglandin biosynthesis in human endometrial explants. Contraception 2019: 99: 61–66.
- Sabatini R., Orsini G., Cagiano R. i wsp. Noncontraceptive benefits of two combined oral contraceptives with antiandrogenic properties among adolescents. Contraception. 2007; 76 (5): 342–347.
- Zahradnik H.P. Belara1 – a reliable oral contraceptive with additional benefits for health and efficacy in dysmenorrhoea. The European Journal of Contraception and Reproductive Health Care 2005; 10 (Suppl 1): 12–18.